راهنمای جامع انتخاب محیط کشت ویروسی
کشت ویروسی یک تکنیک آزمایشگاهی است که در آن نمونههای ویروسی به کمک ردههای سلولی مختلف و تخصصی تلقیح داده میشوند. علت این امر آزمایش ویروس برای سنجش توانایی آلوده کردن (عفونت زایی و یا هر گونه فعالیت غیر متعارف) میباشد. اگر سلولها تغییرات سیتوپاتیک (Cytopathic effects) نشان دهند کشت مثبت است.
فهرست
تعریف اثرت سیتوپاتیک
به طور خلاصه به تغییراتی که پس از آلوده شدن به ویروس در سلول رخ میدهد (و معمولاً غیرقابلبازگشت است)، اثرات سیتوپاتیک (CPE) گفته میشود. برای مثال به طور معمول غشا صاف است اما در سلول آلوده به ویروس ممکن است چروکیده شود.
به بیان دیگر، اثر سیتوپاتیک یک آسیب غیر لیتیک (Non-lytic) است که ویروسها به سلولها وارد میکنند. این اثرات در ظاهر و اثر تخریب خود متفاوت هستند. بهطورکلی ویروسها را میتوان به دو گروه کشنده لیتیک (و غیر کشنده) غیر لیتیک دستهبندی نمود.
اما باید این نکته را هم مدنظر داشته باشیم که برخی از ویروسها باعث ایجاد تغییرات ظاهری در سلول آلوده نمیشوند. سلولهایی که ویروس در آنها نهفته و غیرفعال است، علائم کمی از عفونت را نشان میدهد و معمولاً به طور طبیعی کار میکنند. این امر باعث عفونت پایدار میشود و ویروس اغلب برای ماهها یا سالها خنثی باقی میماند. این نوع عفونت اغلب در مورد ویروسهای هرپس اتفاق میافتد.
عفونت های ویروسی نهفته در انسان شامل:
هرپس سیمپلکس (herpes simplex)، واریسلا زوستر (varicella zoster)، اپشتین بار (Epstein-Barr)، سیتومگالوویروس انسانی (human cytomegalovirus)، آدنوویروس (adenovirus) و سارکوم کاپوزی (Kaposi's sarcoma)
شیوه کلی کشت ویروسی
بهطورکلی دو نوع کشت ویروسی سنتی و shell vial مرسوم است که در ادامه به برسی ویژگیهای هر یک میپردازیم.
روش کشت shell vial culture
برای تشخیص سریع ویروس ها در شرایط آزمایشگاهی از روش shell vial culture استفاده میشود و نمونه ویروسی بر روی یکلایه سلولی سانتریفیوژ میشود و رشد ویروس با روشهای تشخیص آنتیژن اندازهگیری میشود. این امر زمان تشخیص ویروسهایی با رشد آهسته مانند سیتومگالوویروس (Cytomegalovirus) را بسیار کاهش میدهد. علاوه بر این، مرحله سانتریفیوژ در کشت shell vial، حساسیت این روش را افزایش میدهد زیرا پس از سانتریفیوژ، ذرات ویروسی نمونه دقیقاً در مجاورت سلولها قرار میگیرند و مدت زمان لازم برای تلقیح رده سلولی را تا حد زیادی کاهش میدهند. (از 5 تا 10 روز در روش های سنتی به 24 ساعت در روش های جدید.)
هر دو سلولهای گونه انسانی و میمون در کشت سنتی ویروس و هم در کشت shell vial استفاده میشوند اما مهمترین ردههای سلولی که به طور گسترده برای تشخیص ویروسی استفاده میشوند، سلولهای اولیه کلیه میمون رزوس (RhMK)، سلولهای اولیه کلیه خرگوش، MRC-5، فیبروبلاستهای پوست ختنهگاه انسان، HEp-2 و A549 هستند.
روش سنتی کشت ویروسی
هر روشی بهغیراز shell vial culture، ویروس کشت داده شود (برای مثال کشت در تخممرغ)، جز کشت سنتی در نظر گرفته میشود. باید در نظر داشت که بهطورکلی کشت ویروسی سنتی با کشت shell vial جایگزین شده است.
با استفاده از روشهای سنتی کشت سلولی، میتوان انواع ویروسها را در ردههای سلولی مختلف شناسایی کرد. با این حال، زمان طولانی مورد نیاز برای انکوباسیون و مشاهده CPE معایب قابل توجهی است. علاوه بر این، هزینه بالای مربوط به خرید و نگهداری سلول های تک لایه مختلف محدودیت دیگری به شمار میاید.
انواع ویروسهای انسانی که با کشت ویروسی قابلشناسایی هستند
گونه های آدنوویروس (Adenovirus)، سیتومگالوویروس (cytomegalovirus)، انتروویروس (enterovirus)، ویروس هرپس سیمپلکس (herpes simplex virus)، ویروس آنفلوانزا (influenza virus)، ویروس پاراآنفلوآنزا (parainfluenza virus)، راینوویروس (rhinovirus)، ویروس سنسیشیال تنفسی (respiratory syncytial virus)، ویروس واریسلا زوستر (varicella zoster virus)، سرخک (measles)و اوریون (mumps) به کمک روش ایمونوفلورسانس (immunofluorescence) شناسایی میشوند، بهاستثنای سیتومگالوویروس و راینوویروس که شناسایی آنها در کشت ویروسی توسط اثرات سیتوپاتیک (cytopathic) تعیین میشود.
اثر سیتوپاتیک رده سلولی آلوده شده به CMV :
اثر سیتوپاتیک اولیه (ECE) شامل گرد شدن فیبروبلاستهای آلوده است، در حالی که اثر سیتوپاتیک دیررس (LCE) با ظهور اجسام انکلوژن داخل سیتوپلاسمی و داخل هستهای دانهدار یا متراکم و همچنین با افزایش حجم سلول مشخص میشود.
ویروس هایی که معمولاً از نمونه های بالینی جدا می شوند
| No | نمونه | ویروس |
|---|---|---|
| 1 | Blood | CMV, enteroviruses ,HSV, VZV |
| 2 | CSF and CNS tissues | Enteroviruses, mumps virus, HSV, CMV |
| 3 | Dermal lesions | HSV, VZV, adenovirus, enteroviruses |
| 3 | Eye | HSV, VZV, adenovirus, enteroviruses, CMV |
| 4 | Genital | HSV, CMV |
| 5 | Mucosal | HSV, VZV |
| 6 | Oral | HSV, VZV |
| 7 | Rectal | HSV, VZV, enterovirus |
| 8 | Respiratory tract (upper) | Adenovirus, rhinovirus, influenza, parainfluenza, enteroviruses, RSV, reovirus, HSV |
| 9 | Respiratory tract (lower) | Adenovirus, influenza, parainfluenza, RSV, CMV |
| 10 | Stool | Enteroviruses, adenoviruses |
| 11 | Tissues | CMV, HSV, enteroviruses |
| 12 | Urine | CMV, adenovirus, enteroviruses, mumps |
HSV − Herpes simplex virus / CMV − Cytomegalovirus
VZV − Varicella-zoster virus / RSV − Respiratory syncytial virus
اهمیت کشت بافت در کشت ویروسی چیست؟
کشت بافت ویروسهای حیوانی شامل رشد سلولهای حیوانی در فلاسکها با استفاده از محیطهای مختلف براث و سپس آلوده کردن این سلولها با ویروس است. این روش به شناسایی و تشخیص ویروسها در آزمایشگاه کمک میکند.
مطالعه بیشتر : معرفی انواع محیط کشت سلولی و کاربرد آنها
ترانسفکشن (Transfection) چیست؟
ترانسفکشن فرایند واردکردن مصنوعی اسیدهای نوکلئیک (DNA یا RNA) به سلولها، با استفاده از ابزاری غیر از عفونت ویروسی است. چنین معرفیهایی از اسید نوکلئیک خارجی با استفاده از روشهای مختلف شیمیایی، بیولوژیکی یا فیزیکی میتواند منجر به تغییر ویژگیهای سلول شود و امکان مطالعه عملکرد ژن و بیان پروتئین در بافت سلول را فراهم کند.
ترانسفکشن (Transfection) را میتوان با استفاده از فسفات کلسیم، به روش الکتروپوراسیون (electroporation)، یا با مخلوط کردن یک لیپید کاتیونی با مواد برای تولید لیپوزوم (liposomes) انجام داد که با غشای سلولی ترکیب شده و محموله خود را به داخل انتقال میدهد.
روش نگهداری و انتقال
کشت سلولی از نظر حساسیت به ویروسهای مختلف بسیار متفاوت پاسخ میدهد. ازاینرو بسیار مهم است که اختصاصی ترین محیط کشت ها و رده های سلولی برای یک ویروس خاص استفاده شود.
نکات نگه داری و انتقال ویروس
- سوابها باید در یک ویال حاوی محیط انتقال ویروس (VTM) قرار داده شوند.
- مایعات و بافتهای بدن باید در یک ظرف استریل قرار گیرند.
- نمونه به چندین نوع مختلف کشت سلولی بسته به ماهیت نمونه و تظاهرات بالینی تلقیح شود.
- محیط نگهداری باید بعد از یک ساعت یا صبح روز بعد تعویض شود.
- لولههای تلقیح شده باید در دمای 35-37 درجه سانتیگراد در یک درام چرخان انکوبه شوند. چرخش برای جداسازی ویروسهای تنفسی لازم است و منجر به ظهور زودتر اثرات سیتوپاتیک (CPE) برای بسیاری از ویروسها میشود. اگر از لولههای ثابت استفاده میشود، بسیار مهم است که لولههای کشت طوری قرار گیرند که تکلایه سلول در محیط غذایی غوطهور شود.
دستهبندی ویروسها بر حسب ماده ژنتیکی
ویروس ها را برحسب ماده ژنتیکی اعم از DNA یا RNA و اینکه ساختار آن تک رشته ای یا دو رشته ای، خطی یا دایره ای و قطعه بندی شده یا غیرقطعی (segmented or non-segmented) طبقه بندی میکنند.
ژنوم های ویروسی با توجه به نوع اسید نوکلئیک، اندازه، پیچیدگی و مسیرهای انتقال اطلاعاتی که دنبال می کنند، تنوع فوق العاده ای از خود نشان می دهند. هدف یک ویروس تکثیر خودش است. برای انجام این کار، ویروسها استراتژیهای مختلفی را برای تکثیر ژنوم خود و تولید پروتئینهای ساختاری و کاتالیزوری مورد نیاز برای تشکیل ویروسهای جدید ایجاد کردهاند که به طور خلاصه آنها را بیان میکنیم.
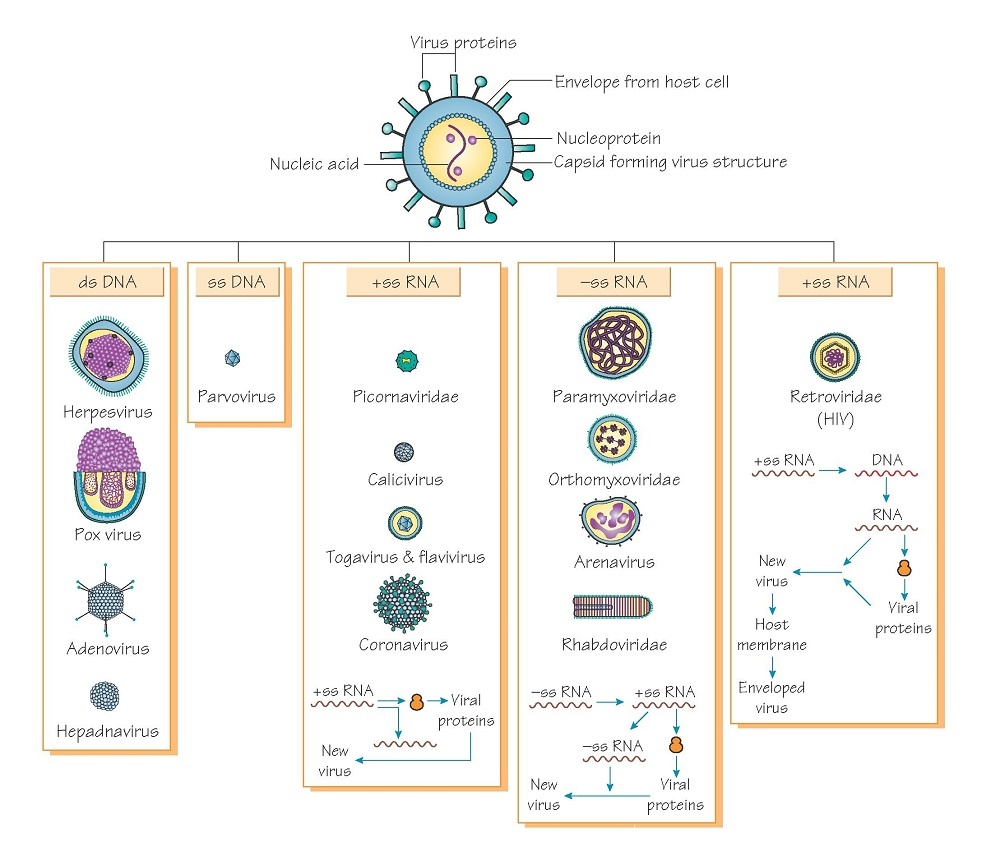
در گونههای مختلف ویروس هر دو نوع اسید نوکلئیک یعنی DNA و RNA یافت میشوند اما در هر ویروس فقط یکی از آنها وجود دارد و هیچ ویروسی به طور همزمان دارای DNA و RNA نیست. در این مورد تنها یک استثنا وجود دارد؛ سیتومگالوویروس (Cytomegalovirus)، نام ویروسی انسانی است که به طور همزمان یک DNA مرکزی و رشته mRNA دارد.
اسید نوکلئیک در گونههای مختلف ویروسها بهصورت تک رشته یا دو رشته است؛ بنابراین در ویروسها اسیدهای نوکلئیک به چهار حالت دو رشته و تک رشته DNA و دو رشته و تک رشته RNA دیده میشوند.
در ویروسهای حیوانی تمام حالتهای رشتههای اسیدهای نوکلئیک دیده میشود اما در گیاهان تنها حالت تک رشته RNA قابلمشاهده است. اکثر باکتریوفاژها هم دارای دو رشته DNA هستند. علاوه بر اینها تک یا دو رشتههای DNA میتوانند بهصورت خطی یا حلقوی باشند.
اندازه ژنوم یا بهاصطلاح وزن نوکلئوتیدها در بین گونههای مختلف میتواند متفاوت باشد. کوچکترین ژنوم که تنها 4 پروتئین را کد میکند درحالی که برزگ ترین ژنوم ویروسی بالغ بر 100 پروتئین را کد میکند. برخی از ویروسها نوکلئوتیدهای غیرطبیعی دارند. بهعنوانمثال، این ویروسها درون ژنوم خود بهجای نوکلئوتید، سیتوزین و یا هیدروکسی متیل سیتوزین دارند.
در ویروسهای RNA دار، این رشتهها بهعنوان رشته مثبت (Plus Strand) یا رشته منفی (Minus Strand) شناخته میشوند. رشته مثبت RNA ویروسی با رشته mRNA یکسان است و میتواند بلافاصله توسط سلول میزبان به پروتئین ترجمه شود. رشته منفی RNA ویروسی، مکمل رشته mRNA است و بنابراین باید ابتدا توسط RNA پلیمراز به رشته مثبت تبدیل شود و سپس مورد ترجمه قرار گیرد.
همه ژنومهای دو رشتهای از جنس RNA و بعضی از ژنومهای تکرشتهای RNA قطعهقطعه هستند و به بخشهای جدا از هم تقسیم میشوند.
هر بخش در یکرشته ممکن است یک پروتئین را کد کند. همچنین بخشهای مختلف معمولاً با هم دیگر در یک کپسید قرار میگیرند. این نکته قابلتوجه است که برای ایجاد عفونت و بیماریزایی همیشه لازم نیست که تمام بخشهای ژنوم یک ویروس درون یک ذره یا کپسید قرار بگیرند.

اشتراک گذاری